Un ejemplo de ensayo de toxicidad utilizando nuestra tecnología:
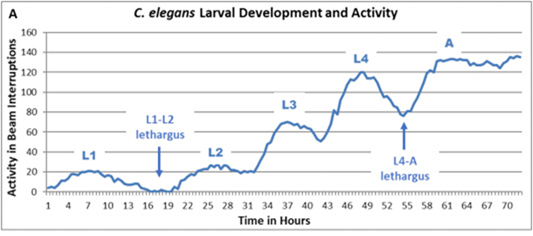
En la publicación de Hunt, «Las pruebas de desarrollo y actividad en C.elegans detectan neurotoxinas del desarrollo de mamíferos» (2018), describe un ensayo novedoso para evaluar la neurotoxicidad del desarrollo (NTD) registrando el tiempo de desarrollo, así como los niveles de actividad en las larvas de C.elegans, Prueba de actividad y Desarrollo en gusanos (wDAT). El desarrollo larvario de C.elegans progresa a través de cuatro etapas distintas que pueden identificarse por el tamaño y la morfología de las larvas. Entre cada una de estas etapas, el gusano en desarrollo entra en un breve período de letargo durante el cual la cutícula se desprende y la alimentación y movimiento se detienen (Figura 1).
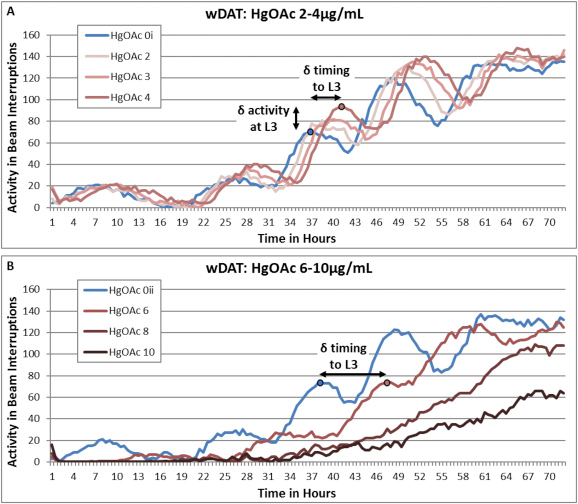
Utilizando el equipo WMicrotracker ONE, los investigadores lograron realizar una evaluación automatizada de los niveles periódicos de actividad e inactividad que les permitió evaluar el progreso del desarrollo de C.elegans a través de las cuatro etapas larvarias y hasta la edad adulta. Los cambios en la altura máxima de la actividad de wDAT en relación con el control indicarían niveles de actividad motora alterados específicos de la etapa de desarrollo de la población. El wDAT es capaz de identificar retrasos en el desarrollo e hiperactividad en presencia de arsénico, plomo y mercurio (figura 2), metales pesados que son neurotoxinas conocidad en el desarrollo humano y que se han asociado con hiperactividad en niños.
Buenas Prácticas de Cultivo de C.elegans:
Un artículo publicado por Piper Hunt en Journal of Applied Toxicology de la División de Toxicología Aplicada (FDA-EE. UU), resalta la utilidad del modelo de C.elegans para una primera búsqueda en pruebas de detección de toxicidad predictiva. El artículo trata sobre el potencial y las limitaciones del modelo animal, así como también describe buenas prácticas de cultivo de C.elegans (BPCCe) que resultan esenciales para garantizar resultados confiables y reproducibles en los ensayos de toxicidad con este nematodo.
“Caenorhabditis elegans es un nematodo pequeño que se puede mantener a bajo costo y manipular mediante técnicas in vitro estándar. A diferencia de los ensayos de toxicidad que utilizan cultivos celulares, las pruebas de toxicidad en C.elegans proporcionan datos de un organismo completo metabólicamente activo con sistema digestivo, reproductivo, endocrino, sensorial y neuromuscular. Se ha demostrado que la clasificación de toxicidad en C. elegans es tan predictiva como la LD50 en rata o la LD50 de ratón. Además, en muchos casos se han observado mecanismos tóxicos de acción conservados entre C.elegans y mamíferos. Estas correlaciones consistentes, hacen posible la inclusión de ensayos utilizando el modelo C.elegans para testeos tempranos de seguridad y como estrategia de pruebas de toxicidad integradas o escalonadas. Aun así, los nematodos por sí solos no pueden reemplazar los datos obtenidos con mamíferos para la evaluación de compuestos peligros».
Según el artículo publicado, «C.elegans utilizados en testeos de toxicidad deben ser mantenidos adecuadamente, con temperatura, concentración de sal y suficiente suministro de nutrientes constante para asegurar resultados confiables y reproducibles (Tabla 1). Las alteraciones, incluso de corta duración, en cualquiera de estas variables podrían conducir a una expresión génica alterada y una respuesta a las toxinas, que podría permanecer durante varias generaciones».
Tabla 1. Factores de estandarización del cultivo de C.elegans para toxicología y BPCCe. (Adaptado de “El modelo C.elegans en testeos de toxicidad- Piper Reid Hunt)
| Factor | Detalle |
| Temperatura | Pequeñas diferencias de temperatura tienen un gran efecto en la tasa de crecimiento, la motilidad, el ciclo de vida, la esperanza de vida y la expresión génica de C.elegans. |
| Humedad | La baja humedad podría alterar el compuesto a testear, la concentración de nutrientes, cuanto menor sea el volumen, mayor será el efecto. |
| pH | Se requiere un pH extremo para alterar la viabilidad de un C.elegans adulto, pero otros criterios de valoración son más sensibles al pH. Se debe determinar el rango de pH apropiado para cada ensayo. |
| Densidad de Gusanos | La expresión génica y el ciclo de vida de C.elegans responden a la disponibilidad de nutrientes y las hormonas secretadas. |
| Sincronización | Larvas L1 de C.elegans pueden obtenerse mediante tratamiento con hipoclorito de hermafroditas grávidas. Los huevos liberados se dejan eclosionar en solución no nutritiva. Después de más de 18 horas en ausencia de nutrientes, la expresión génica se altera, lo que resulta en un desarrollo lento y desincronizado con una mayor resistencia al estrés. |
| Dauers | Las larvas de C.elegans en estadio dauer secretan feromonas, que promueven la conversión al estadio dauer en otras larvas e inducen una mayor resistencia en adultos expuestos a estrés. Esto reduce la tasa de crecimiento aparente medidas por la longitud del gusano y aumentará la viabilidad en presencia de muchas toxinas. |
| Variación genética | Se debe programar el uso de cepas congeladas para evitar la deriva genética. |
| Machos | La no disyunción del cromosoma X da como resultado machos XO. Esto ocurre raramente en la naturaleza y es inducido por toxinas y estrés. Los machos son más pequeños que los hermafroditas XX, lo que resultará en un aparente crecimiento reducido. El apareamiento con machos duplica con creces la progenie por hermafrodita en relación con la autofecundación, por lo que los machos en un cultivo aumentarán la producción reproductiva. |
| Medio sólido vs medio líquido | Cuando el compuesto a testear se mezcla con agar fundido, la verdadera exposición dependerá de muchos factores. La dosificación en medio líquido proporciona una exposición medible, pero limita la prueba a compuestos solubles en agua. |
| E. coli vs Medio Axénico | El medio axénico evita factores que interfieren con la respuesta metabólica del organismo. |
Hunt PR (2017) The C.elegans model in toxicity testing. J. Appl. Toxicol. 37:50–59.
Hunt PR, Olejnik N, Bailey KD, Vaught CA, Sprando RL (2018) C.elegans development and activity test detects mammalian developmental neurotoxins. Food Chem Toxicol 121:583–592
